23.11.2016
Autorzy:
Praktyki:
Specjalizacje:
17.11.2016 opublikowany został zaktualizowany projekt ustawy o zmianie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych.
W dniu 17 listopada br. opublikowany został zaktualizowany projekt ustawy o zmianie ustawy o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych oraz niektórych innych ustaw. Nowa wersja uwzględnia stanowiska wyrażone w trakcie uzgodnień i konsultacji publicznych, które zakończyły się 25 lipca tego roku. Ponadto wraz z aktualizacją projektu Resort Zdrowia przedstawił propozycję szeregu aktów wykonawczych.
W związku z powyższym przedstawiamy Państwu zaktualizowany alert refundacyjny, w którym przeanalizowaliśmy najważniejsze zmiany prawne proponowane we wskazanym projekcie, wskazując na różnice między pierwotną i obecną wersją. W przypadku braku różnic pomiędzy wersjami pozostawiliśmy tekst analizy bez zmian. Ponadto, załączamy do alertu aktualny tekst jednolity ustawy o refundacji.
Analizując zakres wprowadzonych zmian należy wskazać, iż w znacznej mierze mają one charakter porządkowy. Doprecyzowują przyjęte wcześniej założenia, nie zmieniając przy tym zasadniczo całego systemu oraz jego poszczególnych elementów. Zgodnie z wcześniejszymi wyjaśnieniami wszystkie istotne zmiany zostaną zaznaczone w niniejszym tekście.
Głównym celem projektu jest zmiana zasad refundowania wyrobów medycznych i wprowadzenie nowego systemu wzorowanego na mechanizmie refundacji leków. Nowelizacja będzie obejmowała wyroby medyczne wydawane na zlecenie oraz wyroby medyczne stosowane obecnie w ramach świadczeń gwarantowanych. Zgodnie z uzasadnieniem Ministra Zdrowia nowy system ma odpowiadać aktualnemu zapotrzebowaniu na wyroby medyczne oraz zapewnić przejrzystość i racjonalizację wydatków na wyroby medyczne (zarówno płatnika publicznego, jak i świadczeniobiorcy).
W ramach nowego systemu przewidziano kilka etapów prowadzących do objęcia refundacją wyrobów medycznych. Na pierwszym etapie Minister Zdrowia, w drodze rozporządzenia, określi grupy wyrobów medycznych, które będą mogły zostać objęte finansowaniem. Wydzielenie grup wyrobów będzie odbywać się m.in. przy uwzględnieniu wpływu na wydatki płatnika publicznego i świadczeniobiorców (pacjentów). Do czasu wskazania danej grupy wyrobów w rozporządzeniu, zachowany zostanie co do zasady dotychczasowy tryb refundacji.
Dla produktów wyróżnionych w pierwszym etapie możliwe będzie uzyskanie decyzji w przedmiocie objęcia refundacją lub ustalających urzędowe ceny zbytu. Decyzje te wydawane będą w indywidualnych postępowaniach toczących się na podstawie przepisów Kodeksu postępowania administracyjnego. W trakcie postępowania refundacyjnego wnioskodawca będzie zobowiązany wskazać szereg informacji dotyczących m. in. cen wyrobów uzyskiwanych w innych państwach UE i EFTA oraz wziąć udział w negocjacjach dotyczących w szczególności urzędowej ceny zbytu wyrobu. Wydanie decyzji refundacyjnej dla danego wyrobu będzie się wiązało z obowiązkiem stosowania ustalonych w niej sztywnej ceny oraz ustawowej sztywnej marży.
Nowe przepisy wprowadzą ponadto możliwość dopłaty świadczeniobiorcy do wyrobów stosowanych w ramach świadczeń gwarantowanych. Płatnik publiczny będzie refundował wyrób do wysokości limitu finansowania, natomiast powyżej tego limitu pacjent będzie mógł wybrać droższy wyrób oraz dopłacić we własnym zakresie.
Etapy procesu legislacyjnego
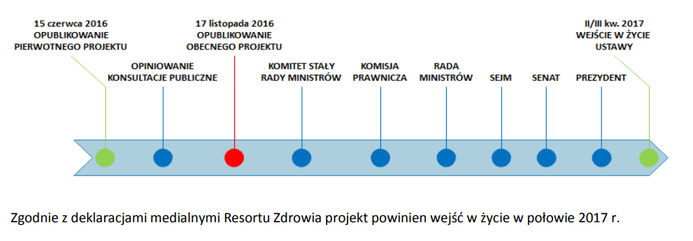
Zgodnie z deklaracjami medialnymi Resortu Zdrowia projekt powinien wejść w życie w połowie 2017 r.
Proces obejmowania refundacją w nowym systemie
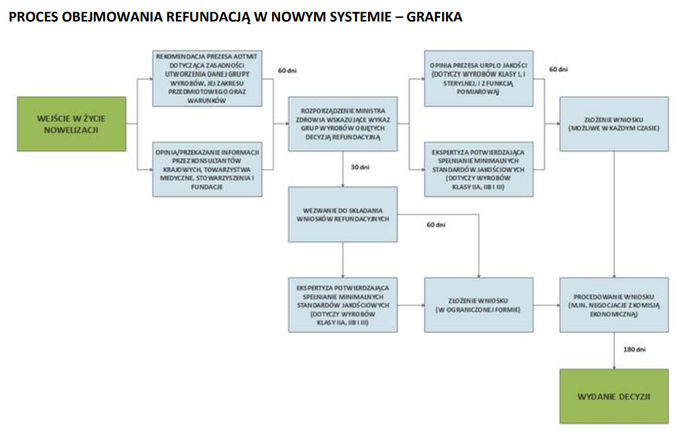
Kluczowe zmiany dla pacjentów
- wprowadzenie możliwości wyboru wyrobu medycznego użytego w ramach świadczenia gwarantowanego,
- prawo do uzyskania za dopłatą wyrobu medycznego stosowanego w ramach świadczeń gwarantowanych, którego cena przekracza limit finansowania,
- możliwość zakupu wyrobów medycznych na zlecenie po cenie urzędowej powiększonej o urzędową marżę.
Kluczowe zmiany dla sklepów medycznych
- obowiązek stosowania marż urzędowych w obrocie wyrobami przysługującymi na zlecenie,
- możliwość dzielenia marży między poszczególne podmioty uczestniczące w obrocie.
Kluczowe zmiany dla świadczeniodawców
- obowiązek rozliczania wyrobów refundowanych po cenach ustalonych w decyzji do limitu finansowania,
- możliwość wykorzystania wyrobów o cenach przekraczających limit finansowania za dopłatą pacjenta,
- możliwość kształtowania ostatecznej ceny wyrobu w ramach maksymalnej marży urzędowej,
- obowiązek nabycia wybranego wyrobu na potrzeby konkretnego pacjenta, w razie wybrania przez niego wyrobu, którego cena przekracza limit finansowania,
- możliwość pobrania od pacjenta „zaliczki” na nabycie wybranego wyrobu medycznego.
Kluczowe zmiany dla producentów
- ustalenie urzędowej ceny zbytu danego wyrobu w decyzji Ministra Zdrowia,
- konieczność wnioskowania o objęcie konkretnych wyrobów refundacją,
- obowiązek stosowania urzędowych cen zbytu również poza systemem refundacji,
- włączanie wyrobów do grup limitowych, w których limit finansowania zostanie oparty na cenie jednego z produktów, uwzględniając cenę, obroty oraz zapotrzebowanie.
Wykaz producentów objętych nową regulacją
- Minister Zdrowia w drodze rozporządzenia będzie sukcesywnie wskazywał grupy wyrobów medycznych, które zostaną objęte decyzją administracyjną, a tym samym będą refundowane na nowych zasadach. W tym zakresie projekt z 27 października br. nie wprowadził zasadniczych zmian, zamiast tego Minister Zdrowia przedstawił propozycję treści rozporządzenia wraz z załącznikiem – wykazem grup wyrobów dla których może być wydana decyzja refundacyjna.
- Zgodnie z nowym projektem Minister Zdrowia w rozporządzeniu będzie wskazywał również minimalne standardy jakościowe, uwzględniając klasę, rodzaj wyrobów, parametry techniczne, właściwości, przewidziane zastosowanie wyrobu medycznego, oraz skuteczność i bezpieczeństwo stosowania we wskazaniach określonych stanem klinicznym pacjenta.
- Przed wydaniem rozporządzenia Minister Zdrowia będzie zlecał Prezesowi AOTMiT przygotowanie rekomendacji w zakresie zasadności utworzenia danej grupy wyrobów, jej zakresu oraz warunków dotyczących wskazań czy świadczeń w ramach których stosowane są wyroby. W uzasadnieniu Prezes AOTMiT będzie musiał przedstawić dowody na wskazane wnioski oraz wpływ na wydatki płatnika publicznego oraz świadczeniobiorców.
- Rekomendacja przygotowywana jest w oparciu o dane dotyczące dotychczasowej refundacji przekazane przez Prezesa NFZ, w razie konieczności Prezes AOTMiT może zwrócić się o udzielenie informacji do konsultantów w odpowiedniej dziedzinie medycyny.
- Ponadto, dzięki przepisom wskazanym w nowym projekcie, w celu uzyskania informacji niezbędnych do określenia minimalnych standardów jakościowych dla grup wyrobów oraz opinii o zasadności wskazania danej grupy, Minister Zdrowia może wystąpić do następujących podmiotów:
- konsultantów krajowych w danej dziedzinie medycyny;
- towarzystw naukowych o zasięgu krajowym;
- stowarzyszeń lub fundacji, których celem statutowym jest ochrona praw pacjenta.
- Wydzielenie grup wyrobów będzie odbywać się przy uwzględnieniu dostępności do świadczeń gwarantowanych, koncentracji rynku, konkurencyjności cenowej, jak również wpływu na wydatki płatnika publicznego i świadczeniobiorców. Zgodnie z zapowiedziami, w pierwszej kolejności refundacją zostaną objęte soczewki, protezy, stenty, pieluchomajtki.
- Nastąpi również modyfikacja wyceny wyrobów medycznych stosowanych w ramach świadczeń gwarantowanych. Z taryfy świadczenia zostanie wyodrębniony koszt wyrobu. Zatem oddzielnie finansowane będzie świadczenie i wyrób medyczny stosowany w ramach świadczenia.
- Dla grup wyrobów wskazanych w rozporządzeniu planowane jest wprowadzenie możliwości uzyskania decyzji o objęciu refundacją i ustaleniu urzędowej ceny zbytu (w przypadku wyrobów wydawanych na zlecenie) lub decyzji o ustaleniu urzędowej ceny zbytu (w przypadku wyrobów stosowanych w ramach świadczeń gwarantowanych).
- Według ustawowej definicji grupa wyrobów medycznych obejmuje zbiór wyrobów medycznych o tym samym lub podobnym przewidzianym zastosowaniu lub o wspólnej technologii, co pozwala na zaliczenie ich do tego samego rodzaju, bez uwzględniania ich specyficznych właściwości.
Ważne! Mimo że nowa regulacja może dotyczyć wszystkich wyrobów medycznych, to Minister Zdrowia będzie określał, które grupy produktów zostaną objęte nową regulacją.
Wezwanie do udziału w postępowaniu refundacyjnym
- W przypadku objęcia decyzją nowej grupy wyrobów medycznych Minister Zdrowia będzie wzywał wytwórców, autoryzowanych przedstawicieli, dystrybutorów lub importerów, których wyroby były stosowane w dniu wejścia w życie rozporządzenia, do udziału w postępowaniu refundacyjnym. Zakres informacji przedstawianych w odpowiedzi na wezwanie będzie ograniczony w stosunku do informacji zawartych w standardowym wniosku refundacyjnym.
- Informacja o wezwaniu publikowana będzie na stronie Ministerstwa Zdrowia, a wniosek będzie mógł również złożyć podmiot, który nie został wezwany, a jego wyroby były dotychczas stosowane. Do czasu objęcia danej grupy wyrobów decyzją administracyjną, zachowane zostaną dotychczasowe zasady refundacji.
Procedura wydania decyzji
- Postępowanie refundacyjne będzie wszczynane w momencie złożenia odpowiedzi, składanej w związku ze wskazanym powyżej wezwaniem (w ograniczonej formie) lub wniosku składanego w dowolnym terminie.
- Wniosek będzie obejmował w szczególności wskazanie proponowanych warunków refundacji, zobowiązanie wnioskodawcy do zapewnienia ciągłości dostaw wraz z określeniem rocznej wielkości dostaw w ujęciu miesięcznym, jak również informacji dotyczących cen wyrobu uzyskiwanych na terytorium RP oraz pozostałych krajów członkowskich UE i EFTA w ciągu ostatnich 12 miesięcy. Złożenie wniosku podlega opłacie (maksymalnie 10 tys. zł), która została dookreślona w projekcie rozporządzenia Ministra Zdrowia.
- Zestawienie opłat w postępowaniu refundacyjnym znajduje się na końcu niniejszego dokumentu.
- W przypadku wyrobów wymagających indywidualnego dopasowania, do wniosku należało będzie dołączyć projekt warunków stosowania wyrobu medycznego w ramach procedury jego doboru. Opis procedury doboru będzie tworzony przez Ministra Zdrowia i dołączany również do obwieszczenia zawierającego wykaz wyrobów refundowanych.
- W nowym brzmieniu projektu nowelizacji – podobnie jak w pierwotnym – w złożonym wniosku ani decyzji nie ma mowy o liczbie jednostkowych wyrobów medycznych przysługującej świadczeniobiorcy w danym okresie użytkowania – kategoria ta pojawia się dopiero na etapie obwieszczenia. Można zatem uznać, że stanowi przedmiot arbitralnej oceny Ministra Zdrowia.
- Dla wyrobów klasy I, I sterylnej albo I z funkcją pomiarową przed złożeniem wniosku konieczne będzie uzyskanie opinii Prezesa URPL o jakości wyrobu medycznego. Wniosek o wydanie opinii podlega opłacie (maksymalnie trzykrotność minimalnego wynagrodzenia za pracę), która została wskazana w rozporządzeniu Ministra Zdrowia.
- W pierwotnej wersji projektu dla wskazanych klas wyrobów również należało uzyskać opinię Prezesa URPL, ale miała ona dotyczyć spełnienia wymagań zasadniczych. Wskazana zmiana wydaje się być zmianą dość powierzchowną – bowiem poza nazwą, większość elementów nie uległa znaczącym zmianom. Procedura wydania opinii oraz działania podejmowane przez Prezesa URPL są dość podobne.
- Wśród istotnych zmian należy wskazać, iż Prezes URPL nie będzie mógł żądać dostarczenia próbek oraz zlecać ich badań lub weryfikacji. Ponadto obniżona została maksymalna opłata za wydanie opinii – z siedmiokrotności minimalnego wynagrodzenia za pracę do trzykrotności.
- Wśród istotnych zmian wprowadzonych w obecnym projekcie należy wskazać obowiązek załączenia ekspertyzy potwierdzającej spełnienie minimalnych standardów jakościowych (wskazanych w rozporządzeniu) dla wszystkich wyrobów klasy innej niż I. Przepisy nie precyzują jednak kto ma wydawać taką ekspertyzę ani jej treści np. w zakresie uzasadnienia przedstawionych w niej wniosków.
- Wnioski dotyczące produktów nieposiadających refundowanego odpowiednika, w których uzasadnieniu podane zostaną argumenty związane z efektem zdrowotnym, dodatkowym efektem zdrowotnym lub kosztem ich uzyskania przekazywane będą do Prezesa AOTMiT w celu przygotowania analizy weryfikacyjnej Agencji, stanowiska Rady Przejrzystości oraz rekomendacji Prezesa.
- Złożenie wniosku, jak i analiza weryfikacyjna będą podlegały opłacie (w pierwszym przypadku do 10,5 tys. zł natomiast w drugim będzie to maksymalnie 150 tys. zł), która została wskazana w projekcie rozporządzenia Ministra Zdrowia. Powyższy obowiązek nie dotyczy wniosków skierowanych w związku z wezwaniem Ministra Zdrowia do udziału w postępowaniu refundacyjnym.
- W tym miejscu warto wskazać, iż zmianie uległa definicja odpowiednika. Wcześniejsze brzmienie tego przepisu wskazywało, iż jest to wyrób medyczny mający takie samo przewidziane zastosowanie oraz właściwości. Według nowej definicji celem ustalenia czy dane wyroby medyczne są swoimi odpowiednikami będzie brana pod uwagę również porównywalna skuteczność i zbliżone bezpieczeństwo stosowania.
- W trakcie postępowania refundacyjnego odbywać się będą negocjacje z Komisją Ekonomiczną dotyczące warunków objęcia refundacją, w trakcie których ustalana jest m.in. urzędowa cena zbytu oraz instrumenty dzielenia ryzyka.
- Wniosek powinien być procedowany nie dłużej niż 180 dni. Zakończeniem postępowania refundacyjnego będzie wydanie przez Ministra Zdrowia decyzji refundacyjnej zawierającej wskazanie urzędowej ceny zbytu. Decyzja pozytywna będzie wydawana na okres do 5 lat, natomiast wyrób objęty finansowanie zostanie wpisany do obwieszczenia refundacyjnego. Możliwe jest również wydanie decyzji odmownej, od której wnioskodawca będzie mógł odwołać się zgodnie z przepisami Kodeksu Postępowania Administracyjnego w terminie 14 dni od dnia doręczenia decyzji.
Ważne! Złożenie wniosku refundacyjnego będzie wiązało się z obowiązkiem uiszczenia szeregu opłat. Z tego obowiązku zwolnione zostaną wyroby objęte wezwaniem.
Poziomy odpłatności
- W przypadku wyrobów medycznych wydawanych na zlecenie objętych decyzją refundacyjną Minister Zdrowia proponuje następujące poziomy odpłatności: bezpłatnie, 10%, 30%, 50%. Natomiast wyroby medyczne stosowane w ramach świadczeń gwarantowanych objęte decyzją uzyskają odpłatność bezpłatnie.
- W przypadku wskazanych poziomów odpłatności dla wyrobów medycznych dostępnych na zlecenie, z wyjątkiem wyrobów dostępnych bezpłatnie, obowiązujące przepisy uzależniają przypisanie danego wyrobu od długości jego stosowania. Natomiast poziom odpłatności bezpłatnie będzie przypisywany wyrobom stosowanym w wybranych wskazaniach:
- chorobach nowotworowych,
- upośledzeniu umysłowym,
- zaburzeniu rozwojowym,
- przy wskazaniach ultrarzadkich,
- chorobach układu nerwowego,
- trwałym uszkodzeniu ośrodkowego układu nerwowego,
- wyłonionej stomii.
Dodatkowo poziom odpłatności bezpłatnie będzie przysługiwał w przypadku dzieci do ukończenia 18. roku życia oraz kobiet ciężarnych.
- Co istotne przypisana powyżej odpłatność nie stanowi całości kosztów, które będzie w wielu przypadkach ponosił pacjent. Wyroby medyczne objęte refundacją zgodnie z nowymi regulacjami będą dostępne za jedną z wskazanych odpłatności ustawowych jedynie do limitu finansowania.
- W przypadku kiedy cena detaliczna danego wyrobu będzie wyższa niż aktualny limit finansowania będzie konieczna dopłata pacjenta wynosząca różnicę między ceną a limitem. W ten sposób nawet dla wyrobów dostępnych w kategorii odpłatności „bezpłatnie” możliwe są dodatkowe koszty dla pacjenta.
Ważne! Wyroby na zlecenie będą wydawane za odpłatnością ustawową powiększoną o dopłatę pacjenta jeżeli cena produktu przekracza wysokość limitu finansowania.
Grupy limitowe
- Wyroby medyczne będą kwalifikowane do grup limitowych tworzonych przy zastosowaniu kryteriów obejmujących: te same wskazania odnoszące się do stanu klinicznego, ten sam zakres zastosowania, podobną skuteczność i właściwości lub parametry techniczne oraz koszt uzyskania podobnego efektu zdrowotnego lub dodatkowego efektu zdrowotnego (jeżeli jest możliwy do określenia.
- W przypadku wyrobów na zlecenie podstawę limitu finansowania w danej grupie będzie stanowiła najwyższa spośród najniższych cen detalicznych za jednostkę wyrobu medycznego, który dopełnia 25% obrotu ilościowego zrealizowanego w tej grupie limitowej w miesiącu poprzedzającym o 3 miesiące ogłoszenie wykazu wskazującego wyroby objęte decyzja administracyjną.
- Jest to jedna ze zmian, którą postulowaliśmy w trakcie dyskusji publicznej nad projektem przekazanym do konsultacji społecznych. W tym przypadku Resort Zdrowia zrezygnował z pierwotnego planu ustalania limitu finansowania na podstawie deklaracji wskazanych we wniosku refundacyjnym.
- W przypadku wyrobów medycznych stosowanych w ramach świadczeń gwarantowanych podstawę limitu finansowania w danej grupie będzie stanowiła najwyższa spośród najniższych urzędowych cen zbytu za jednostkę wyrobu medycznego, który dopełnia 100% szacowanego zapotrzebowania ilościowego i jakościowego w tej grupie. Przy czym pierwotny projekt wskazywał jedynie na zapotrzebowanie ilościowe.
Urzędowe ceny i marże
- Urzędowa cena zbytu, która zostanie ustalona w decyzji, jak również marże wskazane w ustawie, będą miały charakter:
- cen sztywnych i marż maksymalnych dla produktów wydawanych na zlecenie;
- cen maksymalnych dla produktów wykorzystywanych przy realizacji przez świadczeniodawców świadczeń gwarantowanych.
- Urzędowa cena zbytu będzie nakładana na dany towar. Powinna być zatem stosowana niezależnie od tego czy wyrób wydawany jest w ramach systemu refundacji czy poza nim.
- Co ciekawe, nowy projekt zawiera zmiany w zakresie definicji ceny detalicznej w porównaniu z projektem przekazanym do konsultacji publicznych. Zgodnie z nową propozycją przepisów w przypadku wyrobów medycznych będziemy mieli dwie różne definicje.
- Według pierwszej cenę detaliczną wyrobu medycznego stanowi urzędowa cena zbytu powiększona o urzędową marżę hurtową i urzędową marżę detaliczną oraz należny podatek VAT. Definicja ta dotyczy wszystkich wyrobów medycznych, z wyjątkiem tych dostępnych na zlecenie.
- W drugim przypadku – dla wyrobów dostępnych na zlecenie – będzie to urzędowa cena zbytu powiększona o marżę urzędową oraz podatek VAT.
- Marże urzędowe będą wyliczane na podstawie wzorów wskazanych w ustawie, które prezentuje poniższa tabela:
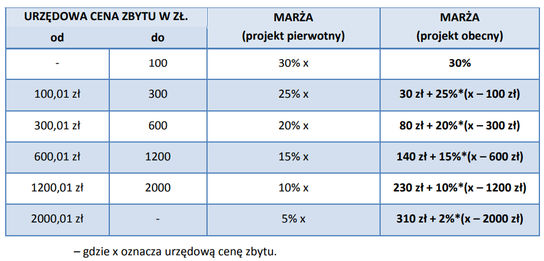
- Poniższy wykres przedstawia różnicę między wysokością marż w obu projektach.
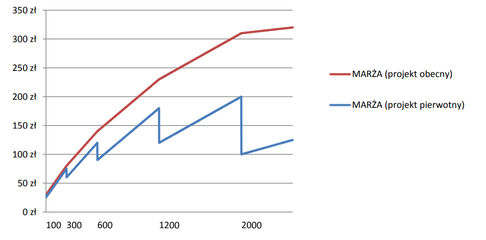
- Stosowanie innych niż ustalone odpłatności i dopłaty do wyrobów medycznych, stosowanie innych niż urzędowe marże na wyroby medyczne, jak również stosowanie cen zbytu netto na wyroby medyczne innych niż ustalone w decyzji refundacyjnej będzie zagrożone karą do 10 mln zł.
- Nowelizacja podobnie jak regulacje lekowe nie precyzuje przy tym poziomu, na jakim stosowana ma być urzędowa cena zbytu, co może rodzić problemy interpretacyjne w szczególności dla wyrobów, którymi obrót prowadzony jest spoza granic Polski, w tym z innych krajów Unii Europejskiej.
Ważne! Ceny i marże będą obowiązywać nie tylko w przypadku nabywania wyrobów przez pacjenta w ramach systemu refundacji, ale również w przypadku sprzedaży tego wyrobu bez współfinansowania z budżetu NFZ.
Dopłaty do wyrobów stosowanych w szpitalu
- Ponadto, wprowadzona zostanie możliwość dopłaty świadczeniobiorcy w przypadku wyrobów stosowanych w ramach świadczeń gwarantowanych. NFZ będzie refundował wyrób do limitu finansowania, natomiast powyżej tego limitu pacjent będzie mógł dopłacić we własnym zakresie.
- Świadczeniodawca będzie mógł również zastosować w ramach świadczeń gwarantowanych wyroby medycznych, dla których nie wydano decyzji o ustaleniu urzędowej ceny zbytu, ale dla których decyzja ta może być wydana, bowiem należą do grupy wskazanej w rozporządzeniu Ministra Zdrowia. Przy czym świadczeniobiorca będzie pokrywał koszt wyrobu medycznego wg ceny nie wyższej niż cena na fakturze zakupu wyrobu, natomiast NFZ będzie rozliczał pozostały koszt zrealizowanego świadczenia po cenie nie wyższej niż wysokość taryfy świadczeń ustalonej przez Prezesa AOTMiT.
- Świadczeniodawca będzie miał obowiązek zapewnić dostępność co najmniej jednego wyrobu o cenie nie wyższej niż limit finansowania, jak również poinformować o innych wyrobach możliwych do zastosowania – w tym o wyrobach refundowanych o cenie wyższej niż limit oraz tych, dla których nie wydano decyzji refundacyjnej.
- Świadczeniobiorca będzie następnie wyrażał zgodę na zastosowanie wybranego wyrobu. Ustawa w tym zakresie wskazuje na procedurę w przypadku pacjentów, którzy nie będą w stanie takiej decyzji podjąć.
- Istotną nowością, która pojawia się w obecnym projekcie jest możliwość zażądania przez świadczeniodawcę od pacjenta uiszczenia zadatku, w przypadku wyboru innego niż mieszczący się w limicie finansowania. W przypadku wyrobu objętego refundacją będzie to kwota do 30% urzędowej ceny zbytu tego wyrobu powyżej limitu finansowania. Natomiast w przypadku wyrobu spoza listy refundacyjnej wartość ta zostanie ustalona przez świadczeniodawcę.
Ważne! Nowy projekt wprowadza nie tylko możliwość wyboru przez pacjenta wyrobu medycznego, który ma zostać zastosowany, ale również pobrania od niego zaliczki na koszt jego zakupu.
Ubezpieczenia zdrowotne
- Ustawa nie ogranicza możliwości, aby koszty nabycia wyrobu medycznego pokrywane przez pacjenta były poniesione przez inne podmioty. W tym zakresie w związku z kosztami związanymi z zastosowaniem lepszych, bardziej dostosowanych do potrzeby danego pacjenta wyrobów, istotną rolę w nowym systemie mogą odgrywać np. prywatni ubezpieczyciele bądź podmioty proponujące pakiety medyczne.
Nowe elementy decyzji
- Wśród elementów decyzji refundacyjnej obowiązujące przepisy wymieniają: dane identyfikujące dany produkt oraz jego wnioskodawcę, kategorię dostępności refundacyjnej, poziom odpłatności, grupę limitową oraz urzędową cenę zbytu (wraz z ewentualnym instrumentem dzielenia ryzyka), a także termin wejścia w życie decyzji oraz okres jej obowiązywania.
- Oprócz elementów decyzji refundacyjnej, które funkcjonują zgodnie z obowiązującymi przepisami obecny projekt postuluje również wprowadzenie dwóch nowych elementów:
- wielkości zadeklarowanych dostaw;
- wskazania klinicznego, w którym lek, środek spożywczy specjalnego przeznaczenia żywieniowego, wyrób medyczny jest objęty refundacją.
Uchylenie decyzji
Decyzja refundacyjna może zostać uchylona w przypadku stwierdzenia braku deklarowanej skuteczności terapeutycznej, ryzyka stosowania niewspółmiernego do efektu terapeutycznego lub podważenia wiarygodności i precyzji oszacowań kryteriów uwzględnionych przy wydaniu decyzji.
Ponadto możliwe będzie uchylenie decyzji jeżeli zobowiązanie dotyczące zapewnienia ciągłości dostaw lub rocznej wielkości dostaw nie zostanie dotrzymane i nastąpi niezaspokojenie potrzeb świadczeniobiorców, jak również w przypadku stwierdzenia wystąpienia zdarzenia lub incydentu medycznego, które doprowadzą lub będą mogły doprowadzić do śmierci lub poważnego pogorszenia stanu zdrowia świadczeniobiorcy.
Ważne! Decyzja w przedmiocie objęcia refundacją może zostać uchylona m.in. w przypadku braku zapewnienia określonej w decyzji wielkości dostaw.
Kary administracyjne
- Nowelizacja zmienia wymiar kary z tytułu naruszenia przepisów dotyczących stosowania odpłatności i dopłat za produkty refundowane oraz stosowania marż i cen urzędowych. Będzie ona mogła być wymierzona w wysokości do 10 mln zł.
- W przeciwieństwie do pierwotnego brzmienia projektu nowelizacji, nowy projekt odnosi się obecnie zarówno do wyrobów medycznych jak i do innych produktów refundowanych. Z ustawy usunięte mają zostać dotychczasowe reguły nakładania kar w wysokości uzależnionej od wartości zrealizowanego obrotu. Omyłkowo jak się zdaje nie skreślono ustępu ustalającego zasady naliczania kary w zależności od tego, czy naruszenia dopuścił się wnioskodawca, podmiot prowadzący obrót hurtowy, czy detalista.
- W mocy pozostawiono również przepis nakazujący uwzględnić przy wymiarze kary okres, stopień oraz okoliczności naruszenia. Oznacza to, że mimo zmiany maksymalnego pułapu kar administracyjnych i uniezależnienia go od obrotów – aktualny pozostaje wymóg aby kara była adekwatna do dokonanego naruszenia.
Tabela opłat
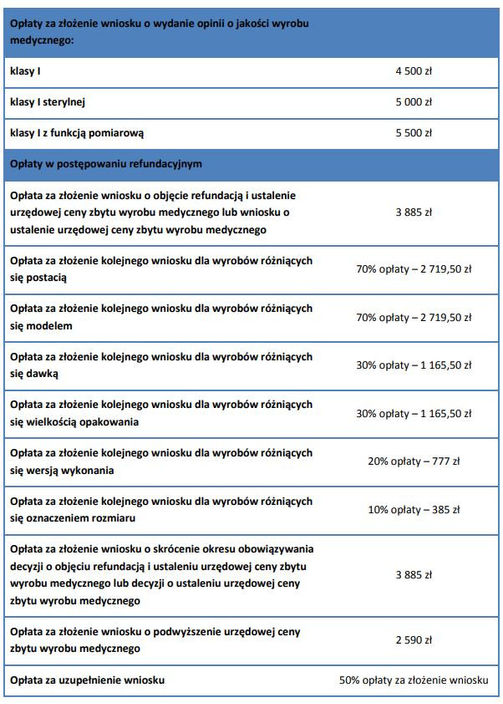
Pełną treść alertu znajdą Państwo w załączonym PDF.